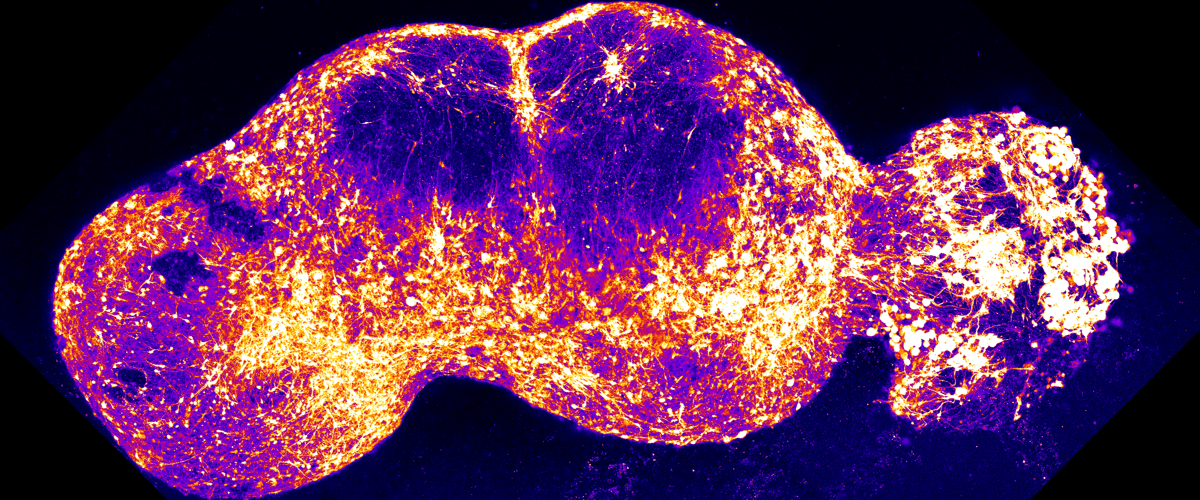
Ученые разработали «сенсорный ассемблоид» — комбинацию из двух и более органоидов, представляющую собой модель болевого пути. Для ее создания клетки кожи человека были перепрограммированы в стволовые клетки. Из этих стволовых клеток исследователи вырастили мини-органы, имитирующие ключевые структуры нервной системы, участвующие в восприятии боли: спинальный ганглий, спинной мозг, таламус и соматосенсорную кору.
Разместив эти органоиды рядом, исследователи три месяца наблюдали, как нейроны из одного кластера прорастали в другой и формировали рабочие нейронные цепи. Стимуляция органоида, представляющего кожные сенсорные нейроны, вызывала электрический импульс, который распространялся по всей цепочке органоидов, подобно тому, как это происходит в нервной системе живого человека.
По сути, ученые с нуля вырастили простейшую систему чувственного восприятия. Созданный ими путь — основная «магистраль» для передачи ощущений вроде прикосновений, тепла и боли.
В теле человека эти сигналы зарождаются в нервных окончаниях кожи, затем передаются в спинной мозг, проходят через таламус (своего рода «коммутатор» мозга) и в конечном итоге достигают соматосенсорной коры, где мы их осознаем.
Для проверки модели команда использовала капсаицин — молекулу, которая придает перцу чили жгучесть. Как и в организме, это вызвало каскад нервных импульсов, зафиксированных методами кальциевой визуализации и электрофизиологии. Сигналы проходили через все четыре мини-органа с определенным ритмом, напоминая обработку сенсорной информации в настоящем мозге. При сравнении ассемблоидов с изолированными органоидами стало очевидно, что только собранная модель демонстрировала последовательное распространение активности по всем четырем областям.
Эта разработка особенно интересна с точки зрения изучения боли. Хроническая боль остается загадкой для науки — животные модели не отражают человеческую физиологию, а прямые исследования ограничены этическими нормами.
В результате врачи вынуждены назначать препараты, разработанные для других целей, от антидепрессантов до опиоидов с их опасными последствиями. Поэтому ученые ищут новые решения.
Возможной целью препаратов может стать белок Nav1.7 в сенсорных нейронах. Изменения в гене SCN9A, отвечающем за этот белок, могут вызывать как повышенную, так и полную потерю болевой чувствительности. Когда команда создала ассемблоиды с гиперактивной версией Nav1.7, нервные клетки стали возбуждаться чаще. Блокировка этого белка, в свою очередь, нарушила передачу болевых сигналов, хотя сами нейроны продолжали работать.
Это указывает на то, что боль возникает не из-за случайных импульсов отдельных клеток, а из-за скоординированной работы всей нервной цепи.
Созданные модели несовершенны — в них нет областей мозга, отвечающих за эмоциональное восприятие боли, и они имитируют раннюю стадию развития мозга, а не взрослую. Тем не менее, возможности их применения очень широки. Ученые уже работают над более сложными моделями, воспроизводящими обратные связи в мозге. Такие органоиды пригодятся для изучения генов, связанных с аутизмом и синдромом Туретта. Стэнфорд уже подал заявку на патент на эту технологию.